Entzündungen in 3D
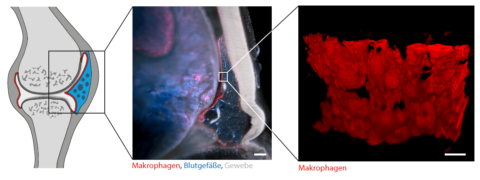
Die genauen Ursachen für chronisch-entzündliche Gelenkserkrankung wie die rheumatoide Arthritis sind weiterhin unzureichend verstanden. Ein Forscherteam des Universitätsklinikums Erlangen und der Universität Erlangen-Nürnberg wählte nun einen neuen Ansatz, um die zugrundeliegenden Mechanismen besser zu verstehen. Mit Hilfe einer eigens entwickelten Technik ist es Stephan Culemann und Dr. Anika Grüneboom aus der Medizinischen Klinik 3 – Rheumatologie und Immunologie – erstmals gelungen, entzündete Gelenke transparent und somit für Licht durchsichtig zu machen. Anschließend haben sie diese mittels dreidimensionaler molekularer Bildgebung untersucht. Dabei haben sie überraschende Einblicke gewonnen, wie unser Immunsystem funktioniert. So zeigte sich unter anderem, dass gesunde Gelenke durch eine sich ständig selbst-erneuernde Membran aus entzündungshemmenden Immunzellen (Makrophagen) ummantelt werden. Während diese Barriere aus Makrophagen unsere Gelenke im Regelfall vor möglichen Attacken des eigenen Immunsystems schützt, kommt es im Rahmen der rheumatoiden Arthritis zu einem Versagen dieses Schutzmechanismus und hierdurch zu einem plötzlichen Einwandern von fehlerhaft aktivierten Immunzellen, welche letztlich die Gelenksentzündung und -zerstörung verursachen. Ihre Ergebnisse haben sie im renommierten Magazin „Nature“ veröffentlicht*.
Ein funktionsfähiges Immunsystem ist zur Abwehr von Krankheitserregern wie Viren und Bakterien überlebensnotwendig. Im Rahmen von chronisch-entzündlichen Autoimmunerkrankungen wie der rheumatoiden Arthritis oder multipler Sklerose kommt es jedoch zu einer fehlgeleiteten (Auto-) Immunreaktion und hierdurch zu einer Entzündung und Zerstörung körpereigener Organe. Durch den kombinierten Einsatz neuer Techniken wie 3-dimensionaler Lichtblatt-Mikroskopie und Einzelzellsequenzierung konnten Erlangener Wissenschaftler nun wichtige Bausteine zum besseren Verständnis dieser Erkrankungen beitragen. Stephan Culemann und Dr. Anika Grüneboom aus der Medizinischen Klinik 3 – Rheumatologie und Immunologie (Direktor: Prof. Dr. Georg Schett) gelang es erstmals den Entzündungsprozess bei rheumatoider Arthritis auf zellulär-molekularer Ebene in 3D nachzuvollziehen. Dieser Ansatz führte zur Identifikation membranartiger Vernetzungen aus speziellen residenten Immunzellen (Gewebsmakrophagen) die funktionstüchtige Gelenke bei gesunden Menschen regelrecht einmauern und so schützen. Molekulare Analysen zeigten, dass sich diese Membranen aus Makrophagen ähnlich einer Darmepithelschicht ständig selbst erneuern. Während Makrophagen bisher im Verdacht standen zur Gelenksentzündung beizutragen, zeigen die aktuellen Analysen, dass Gewebsmakrophagen eigentlich einen wichtigen anti-entzündlichen Schutzmantel um das Gelenk bilden und Entzündungsreaktionen eindämmen können. „Diese Einblicke in die Funktionsweise des Immunsystems werfen nicht nur ein neues Licht auf die komplexe Aufgabenverteilung innerhalb des Immunsystems, sondern zeigen auch neue Therapiemöglichkeiten für chronisch entzündliche Erkrankungen auf“ erläutert Prof. Dr. Gerhard Krönke, der Leiter der Studie, welche soeben in der Zeitschrift „Nature“ publiziert wurde.
* https://www.nature.com/articles/s41586-019-1471-1
Weitere Informationen:
Prof. Dr. Gerhard Krönke
Tel.: 09131/85-34742
gerhard.kroenke@uk-erlangen.de
