Autoimmunität – Koordinierte Mülltrennung durch Fresszellen im Immunsystem
Wissenschaftliche Innovation:
Während Entzündungen treffen Immunzellen nicht nur auf Krankheitserreger, sondern auch auf abgestorbene körpereigene Zellen. Erstmalig konnte gezeigt werden, wie Krankheitserreger von toten Zellen unterschieden werden, sowie deren getrennte Entsorgung durchgeführt wird. Dieser grundlegende Entscheidungsprozess wird von einem in Gewebsmakrophagen identifizierten Enzym (12/15-Lipoxygenase) gesteuert. Dieses Enzym wiederum produziert spezielle Botenstoffe, sog. oxidierte Phospholipide, welche den Abräumprozess durch die unterschiedlichen Immunzellen koordiniert. Fehlt jedoch dieses Enzym so kommt es zu einer gestörten Entsorgung toter Zellen und einer Autoimmunerkrankung.
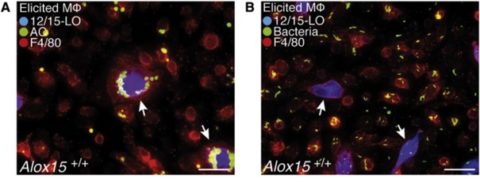
Es konnte nachgewiesen werden, dass tote körpereigene Zellen durch eine spezialisierte Untergruppe von Fresszellen entsorgt werden. Diese Gewebsmakrophagen besitzen die Fähigkeit zur spezifischen Entsorgung von toten Zellen und verhindern somit einen Zugriff von anderen Teilen des Immunsystems auf deren Überbleibsel. Bakterien und andere Krankheitserreger werden jedoch gleichzeitig durch Entzündungszellen (Monozyten) erkannt und aufgenommen, ein Prozess der eine spezifische Immunreaktion zur Folge hat. Damit vollzieht unser Immunsystem innerhalb von Entzündungen und Infektionen frühzeitig eine Form der „Mülltrennung“. Dies dient einerseits der spezifischen Bekämpfung von Krankheitserregern, andererseits der Vermeidung einer Autoimmunreaktion bzw. der Aufrechterhaltung der immunologischen Toleranz. Neben der Identifikation dieser „immunologischen Mülltrennung“ und der daran beteiligten Untergruppen von Immunzellen, konnten auch die zugrunde liegenden molekularen Mechanismen aufgedeckt werden. Während dieser Mechanismus wesentlich zur Aufrechterhaltung der immunologischen Toleranz zu sein scheint, ist diese Oxidation im Laufe des Lebens Hauptursache zur Entstehung von Arteriosklerose sowie Gefäßverkalkung und letztlich für Herzinfarkt und Schlaganfall.
Hintergrund:
Tagtäglich steht unser Immunsystem vor der schwierigen Aufgabe, zwischen schädlichen Mikroorganismen und harmlosen Überresten körpereigener Zellen zu unterscheiden. Die Konsequenzen dieses Entscheidungsprozesses sind weitreichend, da eine Immunreaktion gegen Mikroorganismen für eine lang anhaltende und schützende Immunität benötigt wird. Eine derartige Immunreaktion gegen körpereigene Zellen kann jedoch zu einer lebensbedrohlichen Autoimmunerkrankung führen.
Im Laufe von Entzündungsprozessen bekämpfen Immunzellen nicht nur Krankheitserreger, sondern treffen auch auf abgestorbene körpereigene Zellen. Um eine fehlgerichtete Immunreaktion gegen solche toten Zellen und damit zur Selbstzerstörung und die Entstehung einen Autoimmunerkrankung zu verhindern, müssen diese getrennt „entsorgt“ werden.
Publikation: Uderhardt S, Herrmann M, Oskolkova OV, Aschermann S, Bicker W, Ipseiz N, Sarter K, Frey B, Rothe T, Voll R, Nimmerjahn F, Bochkov VN, Schett G, Krönke G. 12/15-lipoxygenase orchestrates the clearance of apoptotic cells and maintains immunologic tolerance. Immunity. 2012 May 25;36(5):834-46.